ΚΛΙΝΙΚΕΣ ΕΞΕΤΑΣΕΙΣ
Κληρονομούμενες νόσοι

Τι είναι και πώς κληρονομούνται;
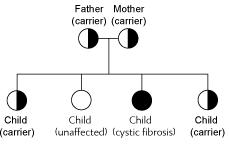
Η πλειοψηφία των γενετικών νοσημάτων που οφείλονται σε ανωμαλίες του DNA, στο ένα ή και στα δύο αντίγραφα ενός γονιδίου (κάθε άτομο φέρει δύο αντίγραφα του ίδιου γονιδίου, ένα μητρικής και ένα πατρικής προέλευσης), κληρονομούνται είτε από τον ένα είτε και από τους δύο γονείς. Άτομα με αλλαγές σε ένα μόνο αντίγραφο του γονιδίου (μητρικής ή πατρικής προέλευσης) συνήθως δεν παρουσιάζουν κλινικά συμπώματα λόγω της παρουσίας του φυσιολογικού αντίτυπου από τον άλλο γονέα και καλούνται «φορείς». Ο παραπάνω τρόπος κληρονομικότητας καλείται υπολειπόμενος. Η παρουσία κλινικών συμπτωμάτων προϋποθέτει την κληρονόμηση και των δύο παθολογικών αντιγράφων ενός γονιδίου. Η πλειοψηφία των γενετικών νοσημάτων υπάγεται σε αυτή την κατηγορία και παραδείγματα αποτελούν η κυστική ίνωση, η α-,/β- θαλασσαιμία, η νωτιαία μυική ατροφία, κ.α.
Μία άλλη κατηγορία γενετικών νοσημάτων κληρονομείται με επικρατή τρόπο, δηλαδή ένα μόνο παθολογικό αντίγραφο γονιδίου αρκεί για την εκδήλωση παθολογικού φαινοτύπου. Παραδείγματα είναι η χορεία του Huntington, ο νανισμός, κ.α.
Τέλος, υπάρχουν γενετικά νοσήματα που κληρονομούνται με φυλοσύνδετο τρόπο μέσω του φυλετικού χρωμοσώματος Χ. Παραδείγματα αποτελούν η αχρωματοψία, η μυική δυστροφία Duchenne, η αιμορροφιλία, κ.α.
Διαγνωστικές Εξετάσεις
Από τη Genomedica παρέχονται οι παρακάτω διαγνωστικές εξετάσεις:
- Κυστική Ίνωση
- α- και β- θαλασσαιμία
- Δρεπανοκυτταρική αναιμία
- Μυική δυστροφία Duchenne
- Νωτιαία Μυική Ατροφία
- Συγγενής κώφωση
- Σύνδρομο του Εύθραυστου Χ
- Οικογενής καρκίνος του μαστού BRCA1 και BRCA2
Αχονδροπλασία
Εάν ένα συγκεκριμένο τεστ δεν αναφέρεται στη λίστα, παρακαλείσθε όπως επικοινωνήσετε με το εργαστήριο. Η Genomedica συνεργάζεται με εργαστήρια αναφοράς του εξωτερικού (GENDIA, www.gendia.net) για σπάνια γενετικά νοσήματα.
Όλες οι διαγνωστικές εξετάσεις είναι διαθέσιμες και για προγεννητικό έλεγχο.
Κυστική Ίνωση
Η κυστική ίνωση αποτελεί την πιο κοινή αυτοσωμική γενετική νόσο στους καυκάσιους με συχνότητα 1/2.500 γεννήσεις. Στην Ελλάδα είναι η δεύτερη πιο κοινή γενετική νόσος, μετά τη β-θαλασσαιμία και τις αιμοσφαιρινοπάθειες, με ποσοστό φορέων πάνω από 5%. Η ασθένεια επηρεάζει αρχικά το αναπνευστικό και το πεπτικό σύστημα και μπορεί να προκαλέσει υπογονιμότητα στους άνδρες ( http://hcd2.bupa.co.uk/fact_sheets/html/Cystic_fibrosis.html για περισσότερες πληροφορίες). Προκαλείται από μία μετάλλαξη στο γονίδιο του ρυθμιστή της διαμεμβρανικής αγωγιμότητας στην κυστική ίνωση (CFTR). Υπάρχουν αρκετές γνωστές μεταλλάξεις του γονιδίου με συχνότερη τη ΔF508. Κλινικά συμπτώματα παρουσιάζουν μόνο τα άτομα που φέρουν και τα δύο παθολογικά αντίγραφα του γονιδίου και όχι οι φορείς των μεταλλάξεων CFTR. Οι γονείς που είναι και οι δύο φορείς μίας μετάλλαξης CFTR, έχουν πιθανότητα 25% να αποκτήσουν παιδί με κυστική ίνωση.
Στη Genomedica παρέχεται η δυνατότητα ελέγχου των:
ΔF508, η συχνότερη μετάλλαξη της κυστικής ίνωσης, η οποία καλύπτει το 53,4% των μεταλλαγών της κυστικής ίνωσης
CF29, περιλαμβάνει 29 πιο κοινές μεταλλαγές, οι οποίες καλύπτουν το 74% των γνωστών μεταλλαγών της κυστικής ίνωσης
Πλήρης ανάλυση (99%) του γονιδίου CFTR
Τα αποτελέσματα δίνονται εντός 7 εργάσιμων ημερών για την εξέταση ΔF508 και CF29 ενώ, για την πλήρη ανάλυση του γονιδίου CFTR απαιτούνται 30 ημέρες (πλήρης κατάλογος διαγνωστικών εξετάσεων). Όλες οι διαγνωστικές εξετάσεις είναι διαθέσιμες και για προγεννητικό έλεγχο.
Τόσο η α- όσο και η β-θαλασσαιμία είναι γενετικά νοσήματα που επηρεάζουν την ποσότητα της αιμοσφαιρίνης η οποία παράγεται στα ερυθρά αιμοσφαίρια (περισσότερες πληροφορίες για τις αιμοσφαιρινοπάθειες στην ηλεκτρονική διεύθυνση, (http://www.hbregistry.org.uk/information/thalassaemia.html).
Οι α-θαλασσαιμίες είναι περισσότερο συχνές στη νοτιο-ανατολική Ασία και στην Κίνα, ενώ οι β-θαλασσαιμίες απαντώνται συχνότερα στους λαούς που κατοικούν γύρω από τη Μεσόγειο. Η β-θαλασσαιμία χαρακτηρίζεται από μειωμένη σύνθεση της αλυσίδας της β-σφαιρίνης λόγω των μεταλλάξεων του γονιδίου β-σφαιρίνης. Σαν αποτέλεσμα αυτού, η αλυσίδα της α-σφαιρίνης βρίσκεται σε περίσσεια και σχηματίζει τετραμερή τα οποία είναι μη διαλυτά και καθιζάνουν εντός των ερυθροκυττάρων, με συνέπεια την πρώιμη διάσπασή τους. Πάσχοντες από β-θαλασσαιμία υπόκεινται τακτικά σε μετάγγιση αίματος.
Οι φορείς της α- ή β – θαλασσαιμίας δεν εμφανίζουν κλινικά συμπτώματα. Οι γονείς που είναι και οι δύο φορείς μίαςμετάλλαξης, έχουν πιθανότητα 25% να αποκτήσουν παιδί με α- ή β-θαλασσαιμία. Στη Genomedica παρέχεται η δυνατότητα ελέγχου των μεταλλάξεων της α- και β-θαλασσαιμίας καθώς και της δρεπανοκυτταρικής αναιμίας. Τα αποτελέσματα είναι διαθέσιμα εντός 5 εργάσιμων ημερών (πλήρης κατάλογος διαγνωστικών εξετάσεων).
Η δρεπανοκυτταρική αναιμία είναι ένα αυτοσωμικό υπολειπόμενο γενετικό νόσημα που οφείλεται σε μεταλλαγή του γονιδίου της β-σφαιρίνης με αποτέλεσμα να αλλάζει το σχήμα των ερυθροκυττάρων από σφαιρικό σε δρεπανοειδές. Λόγω σχήματος, δυσχεραίνεται η κυκλοφορία των ερυθροκυττάρων στα αγγεία. Τα κύτταρα αυτά συσσωρεύονται και παρεμποδίζουν τη ροή του αίματος με συνέπεια την πρόκληση σοβαρών λοιμώξεων καθώς και την καταστροφή ζωτικών οργάνων. Η μεγαλύτερη συχνότητα εμφάνισης της δρεπανοκυτταρικής αναιμίας αλλά και της β-θαλασαιμίας, εντοπίζεται στη Μεσόγειο.
Στη Genomedica παρέχουμε μοριακό έλεγχο για δρεπανοκυτταρική αναιμία και τα αποτελέσματα είναι διαθέσιμα εντός 5 εργάσιμων ημερών (πλήρης κατάλογος διαγνωστικών εξετάσεων).
Τόσο η μυική Δυστροφία Duchenne (DMD) όσο και η ηπιότερη μορφή αυτής, η μυική δυστροφία Becker, οφείλονται είτε σε διαγραφή/διπλασιασμό (σε ~65% των περιπτώσεων) είτε σε σημειακή μεταλλαγή του γονιδίου της δυστροφίνης που εντοπίζεται στη χρωμοσωμική περιοχή Xp21. Η απουσία της παραγωγής της δυστροφίνης οδηγεί σε σταδιακή εξασθένηση και απώλεια μυικού ιστού. Η νόσος προσβάλλει τα αγόρια διότι κληρονομείται με φυλοσύνδετο υπολειπόμενο τρόπο (Χ-linked).
Για περισσότερες πληροφορίες
http://www.muscular-dystrophy.org/about_muscular_dystrophy/conditions/97_duchenne_muscular_dystrophy
Στη Genomedica εφαρμόζουμε την τεχνική του MLPA με την οποία ανιχνεύουμε πιθανή διαγραφή ή διπλασιασμό γενετικών τόπων του γονιδίου της δυστροφίνης. Τα αποτελέσματα είναι διαθέσιμα εντός 10-15 ημερών (πλήρης κατάλογος διαγνωστικών εξετάσεων).
Η νωτιαία μυϊκή ατροφία είναι μία αυτοσωμική νευρομυϊκή ασθένεια που χαρακτηρίζεται από σταδιακή εκφύλιση των κινητικών νευρώνων του προσθίου κέρατος του νωτιαίου μυελού. Τα γονίδια SMN1 και SMN2 εμπλέκονται στη νωτιαία μυϊκή ατροφία. Η απουσία λειτουργικού αντίγραφου SMN1 έχει ως αποτέλεσμα την εκδήλωση της νόσου, ενώ το SMN2 προσδιορίζει τη βαρύτητα της νόσου (τύπου Ι, ΙΙ ή ΙΙΙ).
Για περισσότερες πληροφορίες
http://www.nlm.nih.gov/medlineplus/spinalmuscularatrophy.html
Στη Genomedica εφαρμόζουμε την τεχνική του MLPA με την οποία ανιχνεύουμε την παρουσία ή απουσία του SMN1 γονιδίου και τον αριθμό των SMN2 αντιγράφων. Τα αποτελέσματα είναι διαθέσιμα εντός 10-15 ημερών (πλήρης κατάλογος διαγνωστικών εξετάσεων ).
Η κώφωση είναι η πιο κοινή διαταραχή που παρατηρείται σε γεννήσεις (σε ποσοστό περίπου 1 στα 500 νεογνά) και μπορεί να οφείλεται σε γενετικές αιτίες και μη. Το 80% των περιπτώσεων συγγενούς κώφωσης οφείλεται σε μεταλλαγές ενός γονιδίου και κληρονομείται με αυτοσωμικό υπολειπόμενο τρόπο. Μεταλλαγές στο γονίδιο GJB2 που κωδικοποιεί την πρωτεΐνη connexin-26, ενοχοποιούνται για το 50% των περιπτώσεων συγγενούς κώφωσης. Έχουν βρεθεί πάνω από 200 μεταλλαγές στο γονίδιο αυτό. Η πιο συχνή, είναι η σημειακή έλλειψη 35delG (με συχνότητα 70%). Στην περιοχή της Μεσογείου συναντάται με συχνότητα 1/28.
Στη Genomedica παρέχεται η δυνατότητα ελέγχου:
- 35delG, η συχνότερη μετάλλαξη της συγγενούς κώφωσης, η οποία καλύπτει το 70% των μεταλλαγών. Τα αποτελέσματα δίνονται εντός 5 εργάσιμων ημερών.
- Πλήρης ανάλυση (99%) του γονιδίου GJB2. Τα αποτελέσματα δίνονται εντός 30 ημερών.
- Ανάλυση μεταλλαγών 6 γονιδίων με την μέθοδο array-CGH. Τα αποτελέσματα δίνονται εντός 30 ημερών.
Όλες οι διαγνωστικές εξετάσεις είναι διαθέσιμες και για προγεννητικό έλεγχο.
Το σύνδρομο του εύθραυστου Χ ή και σύνδρομο Martin-Bell είναι μία φυλοσύνδετη γενετική ανωμαλία με κύρια κλινικά χαρακτηριστικά, νοητική υστέρηση, υψηλή αψίδα ουρανίσκου, στραβισμό (οκνηρό μάτι), μεγάλα αυτιά και μακρύ πρόσωπο, μεγάλους όρχεις στα αρσενικά, ήπιο τόνο μυών, πλατυποδία και ήπιες ανωμαλίες των καρδιακών βαλβίδων.
Τα θήλεα μπορούν επίσης να επηρεαστούν αλλά με ελαφρότερη νοητική υστέρηση. Σχεδόν αποκλειστικά μεταβιβαζόμενο από μητέρα προς γιό, επηρεάζει 1 ανά 1.000-2.000 γεννήσεις αρρένων. Το σύνδρομο προκαλείται από μεταλλάξεις στο FMR1 γονίδιο. Το γονίδιο αυτό ρυθμίζει την παραγωγή της πρωτεΐνης FMRP, η οποία πιθανολογείται ότι παίζει κάποιο ρόλο στη δημιουργία συνάψεων μεταξύ των νεύρων. Σχεδόν όλες οι περιπτώσεις Εύθραυστου Χ προκαλούνται από μετάλλαξη σε τμήμα του DNA που αποτελείται από μία CGG επαναλαμβανόμενη αλληλουχία (τριπλέτα) μέσα στο FMR1 γονίδιο. Φυσιολογικά, το τμήμα αυτό του DNA επαναλαμβάνεται από 5 μέχρι 55 φορές περίπου, ενώ σε ασθενείς με σύνδρομο Εύθραυστου Χ η αλληλουχία επαναλαμβάνεται περισσότερες από 230 φορές. Η μεγάλη αυτή επέκταση προκαλεί σπάσιμο στη συγκεκριμένη θέση στο χρωμόσωμα Χ και απενεργοποίηση του FMR1 γονιδίου, παρεμποδίζοντας με τον τρόπο αυτό την παραγωγή της πρωτεΐνης και προκαλώντας την εμφάνιση του συνδρόμου.
Στη Genomedica εφαρμόζουμε την τεχνική του MLPA. Τα αποτελέσματα είναι διαθέσιμα εντός 10-15 ημερών. ( πλήρης κατάλογος διαγνωστικών εξετάσεων).
Οι μεταλλάξεις των γονιδίων BRCA1 και BRCA2 ήταν οι πρώτες μεταλλαγές που συνδέθηκαν αιτιολογικά με την εμφάνιση του καρκίνου του μαστού. Παρόλο που ο οικογενής καρκίνος του μαστού αντιστοιχεί στο 5-10% των συνολικών περιπτώσεων καρκίνων του μαστού, οι γυναίκες με μεταλλάξεις στα γονίδια BRCA1 ή BRCA2 έχουν κατά 50-85% μεγαλύτερο κίνδυνο εμφάνισης της νόσου.
Για περισσότερες πληροφορίες για τον οικογενή καρκίνο του μαστού http://www.cancerhelp.org.uk/type/breast-cancer/about/risks/breast-cancer-genes
Στη Genomedica αναλύουμε πλήρως τα γονίδια BRCA1 και BRCA2 για την εύρεση μεταλλαγών με αλληλούχιση όλου του γονιδίου και MLPA.
Η αχονδροπλασία ή νανισμός είναι ένα αυτοσωμικό επικρατές νόσημα που επηρεάζει το μήκος των άκρων. Σε ποσοστό 75% των περιπτώσεων με αχονδροπλασία έχουν βρεθεί de novo μεταλλάξεις του γονιδίου FGFR3 (fibroblast growth factor receptor gene), που συμβάλλουν στο μη φυσιολογικό σχηματισμό των χόνδρων. Μία διαφορετική μεταλλαγή του γονιδίου FGFR3 προκαλεί μία ηπιότερη μορφή αχονδροπλασίας, γνωστή ως υποχονδροπλασία με κλινικά χαρακτηριστικά τα κοντά άκρα και δυσανάλογο κεφάλι σε σχέση με το υπόλοιπο σώμα.
Στη Genomedica παρέχεται η δυνατότητα ελέγχου των μεταλλάξεων 1138G>C και 1138G>A. Τα αποτελέσματα είναι διαθέσιμα εντός 5 εργάσιμων ημερών (πλήρης κατάλογος διαγνωστικών εξετάσεων ).


